亚洲儿科研究学会(AsianSocietyforPediatricResearch,ASPR)创立于2005年,每年举办一次学术年会,是亚洲儿科领域最高级别的学术会议。第十七届亚洲儿科研究学会学术大会(ASPR2022)由亚洲儿科研究学会、中国医药教育协会、中华医学会儿科学分行和中国医师协会儿科医师分会共同主办,以线上线下相结合的模式于9月17日-18日于成功召开。在由重庆医科大学附属儿童医院新生儿诊疗中心主任史源教授担任主席的“灾害管理”专场,过去五版欧洲RDS指南均担任主要著作者之一的DavidSweet教授首次披露了《2022年欧洲新生儿呼吸窘迫综合征管理指南》的部分精华内容,并透露完整的新版指南预计于年底完成。
呼吸窘迫综合征(RDS)是早产儿常见呼吸系统疾病之一,2007年欧洲围产医学协会组织多名有经验的新生儿科和产科医生,首次发表了欧洲RDS管理指南1,内容涉及产前护理、产房内管理、呼吸支持及肺表面活性物质(pulmonarysurfactant,PS)的使用、药物选择及支持治疗等,依据循证医学证据和医学文献,使用“推荐分级的评估、制订与评价(gradesofrecommationsassessment,developmentandevaluation,GRADE)“这一评级系统反映推荐意见的证据等级。以后每隔3年更新1次,迄今为止共发表了5版指南,对优化早产儿RDS的管理有重要意义,目前该指南不仅被欧洲儿科研究学会所认可,也对指导和规范我国早产儿RDS的管理发挥了一定的作用2,现对DavidSweet教授讲解的《2022年欧洲新生儿呼吸窘迫综合征管理指南》更新要点撷取如下。
产前管理
为使生后存在RDS风险的早产儿获得最佳治疗效果,新生儿医生应加强与产科医生的合作。对于产前管理部分,2022版指南更新要点如下:
妊娠<28-30周有早产风险的孕妇均应转移至具有RDS诊治经验的围产中心(B1)。
妊娠34周内存在早产风险的孕妇至少在分娩前24h给予单疗程产前激素治疗(A1)。
妊娠
表1.2022年与2019年指南3产前管理更新要点
产房内稳定
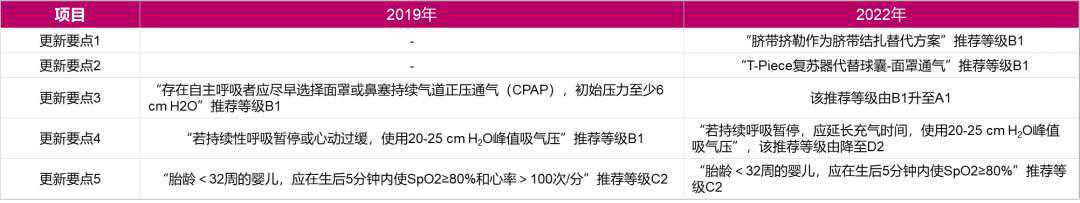
产房内稳定阶段是指对RDS早产儿生后的呼吸转换进行支持4,一是脐带结扎的时机,有研究报道在脐带完整的情况下进行复苏,也有脐带挤勒的相关试验;再者为如何更好地在患儿生后第一口呼吸即提供保障,如新的呼吸支持系统R-PAP、监护设备等;此外还有产房体温控制。针对这些要点,新版指南更新如下:
尽可能延迟脐带结扎至少60s(A1)。仅在脐带结扎不可行时,妊娠28周早产儿可考虑将脐带挤勒作为替代方案(B1)。
建议使用T-组合复苏器(T-Piece复苏器)代替球囊-面罩通气(B1)。
存在自主呼吸者应尽早选择面罩或鼻塞持续气道正压通气(CPAP)(A1)。如出现呼吸暂停给予肺复张,起始压力6/20-25cmH2O(D2)。
复苏时应使用空气氧混合仪控制吸入氧浓度(FiO2)。出生后初始FiO2:胎龄<28周的超早产儿为0.30;胎龄28-31周的极早产儿为0.21-0.30;胎龄≥32周的早产儿为0.21。根据血氧饱和度(SpO2)调整FiO2(B2)。应在生后5分钟内使SpO2≥80%(C2)。
面罩或经鼻塞正压通气无反应的患儿可进行气管插管(A1)。
产房内稳定阶段,胎龄
表2.2022年与2019年产房内稳定阶段更新要点

肺表面活性物质(PS)治疗
对RDS患儿应使用天然动物源性PS(A1)。
LISA是CPAP支持下存在自主呼吸早产儿的首选PS给药方式(A1)。
体重>1.2kg的新生儿可经喉罩气道给予肺表面活性物质(B2)。
若胎龄<30周的早产儿需气管插管稳定时,则应给予PS治疗(A2)。
对RDS患儿应在疾病早期给予抢救性PS治疗(A1)。推荐方案为:当CPAP压力≥6cmH2O、FiO2>0.30,患儿病情进一步恶化,或肺超声提示PS缺乏,即可给予PS治疗(B2)。极度不成熟的早产儿,可考虑较低的FiO2阈值(C2)。
初始剂量200mg/kg的猪肺磷脂用于RDS急救治疗疗效优于100mg/kg的猪肺磷脂或贝拉康坦(A1)。
若存在RDS病情进展的证据,如持续需高浓度氧并排除了其他问题时,可给予第2次、少数情况会给予第3次PS治疗(A1)。
表3.2022年与2019年肺表面活性物质(PS)治疗更新要点

复苏稳定后给氧
在过去几年里,关于目标氧饱和度的定义几乎没有变化。低目标血氧饱和度(85%~89%%~95%)虽降低了严重早产儿视网膜病(ROP)的发病风险,但是同时导致了新生儿病死率的上升及新生儿坏死性小肠结肠炎发病率的增高4。因此将氧饱和度维持在目标范围内及指定ROP的筛查及治疗方案十分重要。指南更新要点如下:
接受氧疗的早产儿,目标饱和度应控制在90%-94%(B2)。
报警范围应设置在89%和95%(D2)。
制定早产儿ROP的筛查及治疗方案(A1)。
表4.2022年与2019年复苏稳定后给氧更新要点
无创呼吸支持
无创通气支持技术目前已广泛应用于新生儿临床,包括经鼻CPAP(NCPAP);无创间歇正压通气(NIPPV);双水平气道正压(BiPAP);加温湿化高流量鼻导管通气(HFNC);无创高频震荡通气(NHFOV)等。为使无创通气临床应用规范化,达到更好的治疗效果2,近年来国内外开展了多项有关无创通气的研究,为我们带来了新的证据。如2017年一篇Cochrane系统综述比较了NIPPV与NCPAP两种无创通气模式,指出在预防再插管或拔管失败方面,NIPPV优于CPAP6。但并不是每个患儿都需要NIPPV,有证据表明HFNC与CPAP效果相当,但鼻损伤风险更小,因此应当了解不同通气模式的优缺点并将其应用于最适合的患儿个体。在无创通气部分,2022版指南更新如下:
所有存在RDS高危风险的新生儿,如胎龄<30周不需要插管复苏的早产儿,出生后应立即使用CPAP或(s)NIPPV(A1)。
对于无创呼吸支持患儿,LISA技术联合早期治疗性使用PS是RDS患儿的优化治疗方案(A1)。
提供CPAP的设备并不重要,但应使用短双鼻孔鼻塞或鼻罩,初始压力为6-8cmH2O(A2)。升级至NIPPV可降低对有创机械通气的需求(A1)。
双水平气道正压(BiPAP)与单独使用CPAP相比并无优势(A2)。若通过呼吸机提供的同步NIPPV可减少有创机械通气需求或拔管后失败再次插管风险,并可能减少BPD(A2)。
经鼻高流量氧疗(HFNC)具有鼻黏膜损伤少的优点可作为CPAP替代治疗,但前提是中心可提供CPAP或NIPPV作为HFNC失败后的营救性治疗(B2)。
表5.2022年与2019年无创呼吸支持更新要点比较
机械通气策略
其他呼吸支持均失败的RDS患儿应使用机械通气(A1),并尽量缩短机械通气时间(B2)。
若使用机械通气(MV),应使用目标潮气量通气或高频振荡通气(A1)。
撤机过程中,的中等程度高碳酸血症是可允许的(B2)。应避免pCO2
一氧化氮(iNO)吸入治疗仅限于伴有肺动脉高压的早产儿,若无反应,则停止治疗(D2)。
推荐使用咖啡因(负荷剂量20mg/kg,维持剂量5-10mg/kg)以助撤机(A1)。所有存在机械通气风险的患儿,如使用无创呼吸支持者,应考虑早期使用咖啡因(C1)。
对机械通气1~2周后仍不能拔管的患儿,可进行短疗程、低剂量或极低剂量并逐渐减量的地塞米松治疗,以促进拔管(A2)。
根据临床判断和疼痛评估选择性使用阿片类药物(D1)。不推荐机械通气的早产儿常规使用吗啡或咪达唑仑注射液(A1)。
表6.2022年与2019年机械通气策略更新要点
综上所述,每次的指南更新都根据最新的临床研究证据,期待《2022年欧洲新生儿呼吸窘迫综合征管理指南》的正式发布。也相信结合最新指南的学习和临床工作的应用,能为我国RDS患儿的救治和管理带来新的指导意义。
专家点评
史源教授
重庆医科大学附属儿童医院新生儿科
参考文献:
1.SweetD,;35(3)175-86
2.石永言,富建华.《2019年欧洲呼吸窘迫综合征管理指南》解读[J].中国实用儿科杂志,2019,34(6):461-516.
3.SweetDG,;115(4)432-450.
4.白瑞苗,将毅等.《2019年欧洲新生儿呼吸窘迫综合征管理指南》推荐意见介绍[J].中国实用儿科杂志,2019,34(16):1201-1203.
5.Abdel-LatifME,;5(5):CD011672.
6.LemyreB,(NIPPV)versusnasalcontinuouspositiveairwaypressure(NCPAP);2(2):CD003212.
排版:管颜青
本文来自【医师报】,仅代表作者观点。全国党媒信息公共平台提供信息发布传播服务。
ID:jrtt
-
长沙地铁行李墙火出圈!一年零盗窃,网友:这才是文明该有的样子
2025-10-10 -
上海网红地打卡全攻略,出片率100%
2025-10-08 -
120万元一针“天价”抗癌药!宁波首例治疗患者重获新生
2025-01-24 -
普乐之声:SDA传奇继续——细说Polk Audio新旗舰 L800 SDA-Pro
2025-04-11